加速人工智能審核─大藥廠及醫療新創公司的AI+新夢
文章發表:2019/04/22
劉依俐
美國食品和藥物管理局(FDA)批准使用人工智能(AI)進行圖像解釋的專有醫療算法的數量正在「迅速擴大」,此係根據2019年1月8日發表在美國自然醫學雜誌(NatureMedicine)上的研究評論文章;此外,加利福尼亞州聖地牙哥研究轉化研究所(The Scipps Research Translational Institute)1的主任和創始人艾瑞克‧塔波(Eric Topol)2所撰寫的研究評論文章指出,FDA發出的AI認證,從2017年每年只有二個,晉升到2018年每月一到兩個;美國FDA專員史考特‧戈特利布(Scott Gottlieb)去年還表示 ,FDA正在積極開發一個新的監管框架,以在人工智能領域促進創新與跟進科技。3
塔波的研究並進一步指出處理深度學習算法(Robust Validation /Deep learning)的監管疏忽是棘手的,因為它目前不允許繼續自動執行功能,而是必須修復軟件,使其行為像非AI診斷系統。4此外,並非單個醫生的錯誤傷害了患者,一旦由AI儀器的診斷失誤,將導致例如大量傷亡的可能性,亦即醫源性風險的可能性是巨大的。這就是為何當前需要進行系統調試、審量、廣泛模擬和驗證及預期審查時的更多原因。有關AI演算法的問題在臨床實踐中被釋放出來。陶波還強調需要更多的證據和強有力的驗證,以說服並支持FDA降低對醫療算法批准的監管要求。5
人工智慧(Artificial Intelligence, AI)法規架構及數位醫療孵化器(Digital Health Incubator )
美國FDA官員認為人工智慧是數位醫療最有希望的工具之一,主張採用預認證(Pre-Cert)方式讓公司可以針對自家產品進行次要的改變,而不需要每次都送新的審查案。在這個潛在因素下,美國FDA正積極的發展全新的法規架構來支持這個領域的創新發展。值得強調的是,美國FDA認為新的法規架構必須有足夠的彈性來跟上這個領域的變化。6
美國FDA官員Scott Gottlieb日前宣布官方「最現代化且彈性的」的數位醫療法規。在過去數個月內,美國FDA已經宣布多項措施(initiatives),用於釐清關於新的數位技術的法規考量。此為一個新的政策,改善包含數種功能的數位健康產品的上市途徑,其中部分產品須符合美國FDA醫療器材法規;另一些產品則不須。新的美國FDA指引目的為明確定出美國FDA將審查哪些軟體功能。如外界預期,FDA的審查焦點將落在關於診斷或治療病患之高風險醫療器材功能的安全與有效性驗證。7此為主力的數位創新行動方案。
預認證1.0(Pre Cert 1.0)將於2018年末開始。2017年9月,美國FDA公佈預認證優先試行計畫(Pre-Cert Pilot Program),聚焦於公司對於設計、測試、驗證、操作、維護的規畫,而不是用產品的特點來決定該公司是否可以獲得預認證。最新消息是美國FDA已釋出這個計畫的作業模型(Working Model)。這個作業模型包含四個組成: 優良證明(excellence Appraisal)、審查確認(Review Determination)、精簡審查(Streamlined Review)、真實世界表現(Real World Performance)。此作業模型被設計成數個疊代的結果,從2018年4月下旬,逐月依據研發者、病患、供應商及社會大眾的輸入(input)更新作業模型,預計將於2018年底推出預認證優先試行規畫第一版(Pre-Cert 1.0),並於2019年繼續優化。於2019年初FDA公佈了其下一階段的數位醫療預先認證「(PreCert)試點計劃」的新測試計劃。PreCert 1.0版的重點是建立軟件作為醫療設備(SaMD)的流程,其中可能包括在FDA當前的權限範圍內使用AI和機器學習算法的軟件功能,關於此,研究學者暨心臟科醫師艾瑞克‧塔波 (Eric Topol)表示處理深度學習算法(Robust Validation /Deep learning)的監管疏忽是棘手的,因為它目前不允許繼續自動執行功能,而是必須修復軟件,使其行為像非AI診斷系統。8
事實上,經過大數據訓練之後,眾多AI 系統便能夠根據大數據及雲端資料庫的演算提供相關的診察判斷,然而多數AI系統在產出質量上仍有一些問題。AI的演算(algorithm)過程都是不透明的黑箱作業,潛藏無法預知的不確定性(uncertainty),一旦啟動運作,即使是AI的設計工程師亦難以預測發生的後果,因此,在醫療機構內從事AI相關業務的人員必須對AI三位一體的概念9加以熟悉。10
FDA還表示,PreCert 1.0版11的重點是建立軟件作為醫療設備(SaMD)的流程,其中可能包括在FDA當前的權限範圍內使用AI和機器學習算法的軟件功能,為其他類型的數字健康工具全面實施PreCert計劃之前可能需要額外的權限,而不僅僅是首創的SaMD(亦即FDA表示在為其他類型的數位醫療器材全面實施PreCert計劃之前可能需要額外的權限)其他部分包括由Viz.ai開發的用於檢測潛在中風的應用程序(app)以及用於幫助患有心房顫動的新Apple Watch中的兩個應用程序。這些應用程序在2018年獲得了FDA的認可。12
2017年,AI的電力驅動設備包括AliveCor的KardiaMobile智能手機應用程序,用於Apple Watch以幫助進行心房顫動檢測和Arterys Oncology 之AI套件。13被認證或許可的AI設備逐步上升趨勢,反映在下表中:
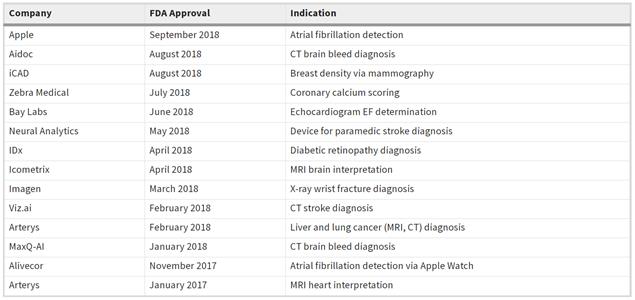
然而,塔波表示,在2017年至2018年間獲得FDA AI認證的大多數公司中,很少有同行業評審。「在經過同行評審的研究中,現實環境中唯一僅僅的前瞻性驗證研究是針對糖尿病視網膜病變、急診室環境中腕關節骨折的檢測、組織學乳腺癌轉移、一小群孩子身上非常小的結腸息肉和先天性白內障。」他指出了一種算法,該算法為去年獲得FDA批准的糖尿病視網膜病變的IDx設備提供支持,作為診所中人工智能的首次前瞻性評估。這種IDx設備是FDA批准的少數AI認證之一。14
與藥物研發及安全通報相關之聲明
美國FDA亦有兩項和藥物研發及安全性相關新措施如下:首先,有鑑於數位健康和處方藥相關的多種應用案例,FDA將發布新的指引說明數位醫療在藥品研發過程扮演角色。其次,目前正在研擬一個新的上市前數位安全計畫(Premarket Digital Safety Program),其目的為在研發中新藥的快速進展的安全通報(Safety Reporting)法規下,能夠有統一的資料標準,以符合電子通報(Electronic Reporting)之要求。新的數位送件流程最終將取代「零散的類比化工作流程」,像是紙本系統。15
台灣藥業近期好事頻傳,台灣聯亞藥廠接獲美國食品藥物管理局(FDA)正式之查廠報告,指聯亞藥新竹廠針劑線通過美國FDA藥品上市前審查查廠,為該公司新竹廠針劑線第三次通過美國FDA查廠。另外,聯亞藥近期也公告,該公司新增劑型(凍晶乾燥注射劑),通過衛生福利部藥品優良製造規範(GMP)查核,認定該廠符合藥物優良製造準則之西藥藥品優良製造規範。16
規模前20大藥廠投資「數位化」創新專業,「AI+新藥」時代來臨
根據美國波士頓TUFTS大學藥物研發中心統計,每個新藥研發成本大約25.58億美元,週期大概10年,其中6~7年都是臨床試驗階段,只有12%的藥物可以通過臨床驗證。
儘管多年來,FDA法規持續變革,希望縮短產業新藥上市的時程,但據2017年的評估顯示,現在開發一款藥物上市的成本高達30億美元,藥物的研發時間至少也需要5年。規模前20大藥廠投資「數位化」僅次於生物製藥。17
而,儘管包括生物製藥和藥廠產品組合高度相關的創新療法,藥物開發仍是藥廠投資基金最為關注的本業領域。但近年來,在「數位化」概念持續倡議之下,大藥廠有相當的比例已往「數位化」進行佈局,只要能為製藥業務提供輔助的數位化工具和平台都到受大藥廠青睞,包括:數位藥物、數位行銷、資料服務等,各種平台服務已經不可計數。
此外,「AI+新藥」工具、大數據資料獲取及應用工具等,能從藥物開發、行銷服務、患者教育到醫患溝通等流程皆為核心的創新專案,也都受到藥廠高度青睞。以AI、機器學習、大數據資料、移動醫療等為代表的「數位化技術」正在重塑醫藥產業,為產業帶來嶄新面貌。
醫藥產業實例
日前宣布美國食品藥物管理局(FDA)批准拜耳(Bayer)18與默沙東(MSD)聯合開發的辨識慢性血栓栓塞性肺高壓(CTEPH)19人工智慧軟體突破性設備指定。此軟體透過胸腔斷層血管攝影(CTPA)深度學習並搭配拜耳的Radimetrics™訊息平台,將顯影劑與註射器和掃描訊息連接起來20,提供放射科醫師重要的見解。21
拜耳開發的智慧Radimetrics™平台能將注射器和掃描訊息連接到Seamlessly Smart™解決方案中,為放射科團隊提供重要見解。這有助於提供更加個性化的護理並符合輻射標準和法規。作為多型態解決方案,Radimetrics™能與現有的IT基礎設施與和放射設備,如核磁共振成像(MRI),電腦斷層掃描(CT),核子醫學(NM),超聲波和乳房X光照相術,無縫集成一致地診斷質量圖像,以協助放射科醫師實踐更安全,更有效率的診斷。
拜耳放射學研究與開發負責人Olaf Weber博士表示,「拜耳期待利用我們在放射學方面的專業知識開發出一種軟體,以支持放射科醫師和治療這種罕見疾病的複雜診斷決策過程,也希望通過批准提高對CTEPH診斷工具的重視,這有助於更可靠地診斷患者從而實現早期治療」 。22
人工智慧帶動醫療的發展後,世界各國各自發揚光大,預期將會發展出更複雜的醫療行為。在可見之未來,醫療行為將大量使用新科技取代傳統人力,AI加乘在新藥研發裡面的能量也必定大發利市、前途可觀。
例如現在常見已透過IBM Watson的輔助,醫師可在遠端診斷、問診,以進行輔助的醫療行為,接著根據病患的需求操作醫療機器人如達文西手臂進行外科手術;FDA審核通過的AI+醫藥數位化應用程式/儀器、加速審核趨勢等等,在此過程中可能衍生爭議的環節將無法以現行以傳統醫療方式所發展出的法令來規範,如何透過資訊通訊科技進行觀察、檢驗、詢問病況,以進行必要的數據判讀、診斷、處方與疾病之治療與預防,提供正確、即時且具有相當品質的醫療照護服務,如在手術過程中過失的認定、甚或是網路系統出問題導致醫療行為有所偏差、出錯的責任歸屬、倫理委員會審議的標準制定等等,都需要法學界經過充分的討論後提出執業準則。
目前固然可以透過利用資訊技術降低日益升高的醫療成本和人力浪費,然在發展過程中,勢必面臨現有法令規範無法適用於之情形。就科技發展的觀點來看,往往法律對科技的限制是過度限制,但就數位醫療這個領域來說,由於牽涉之範圍不僅是個人醫病資料及隱私權相關之問題,更是攸關人身健康及生命安全,因此在立法過程上自是需要更詳盡的考量。臺灣企業因應數位醫療國際法規變革之策略應於安全與隱私保護面和風險管理面做相應調整。
參考文獻
- FDA Speeds Up Artificial Intelligence Approvals, Review Finds
- 美國FDA持續推出數位醫療(Digital Health)新措施。
- 拜耳辨識栓塞性肺高壓AI軟體 獲FDA突破性設備指定。
- FDA Commissioner Continues To Roll Out Digital Health Initiatives。
- Precertification (Pre-Cert) Pilot Program: Milestones and Next。
- FDA grants breakthrough device designation to artificial intelligence software for CTEPH pattern recognition from Bayer and MSD。
註釋
- 斯克里普斯研究所是世界著名的綜合性醫學研究及教育機構。研究領域涵蓋基礎醫學,化學,生物學等方向。總部位於美國加州聖地牙哥市拉霍亞,於2004年在美國弗羅里達州棕櫚灘縣附近的朱庇特鎮建立了其第一個分支。研究人員包括3000餘名科學家,專業技術員,研究生以及其他管理人員。是世界上最大的私立非營利性生物醫學研究機構之一。 返回內文
- Eric Jeffrey Topol(生於1954年),美國心臟病專家,遺傳學家和數字醫學研究員。 返回內文
- FDA speeds up Artificial Intelligence Approals, Review Finds https://www.raps.org/news-and-articles/news-articles/2019/1/fda-speeds-up-artificial-intelligence-approvals-r(2019/3/12) 返回內文
- 同前註。 返回內文
- 同註3。 返回內文
- 美國FDA持續推出數位醫療新措施https://medinnocatalystblog.wordpress.com/2018/06/19/%E7%BE%8E%E5%9C%8Bfda%E6%8C%81%E7%BA%8C%E6%8E%A8%E5%87%BA%E6%95%B8%E4%BD%8D%E9%86%AB%E7%99%82digital-health%E6%96%B0%E6%8E%AA%E6%96%BD/(2019/3/12) 返回內文
- 同前註。 返回內文
- 美國FDA持續推出數位醫療新措施https://medinnocatalystblog.wordpress.com/2018/06/19/%E7%BE%8E%E5%9C%8Bfda%E6%8C%81%E7%BA%8C%E6%8E%A8%E5%87%BA%E6%95%B8%E4%BD%8D%E9%86%AB%E7%99%82digital-health%E6%96%B0%E6%8E%AA%E6%96%BD/(2019/3/12) 返回內文
- 三位一體即融合思維(Idea)、能力(Capality)和倫理(Ethics)於一爐)有基本的認識與了解,才可避免對就醫的顧客造成不良的副作用。在智慧(能)醫院服務的人員不論是直接或間接參與醫療行為者都需要有AI思維,了解AI基本的科學哲學原理,深知AI能力,對應用的潛能有所認識與熟悉,遵守AI倫理,至今尚無國際共識的AI倫理規範與準則,因此,在醫療院所從事AI相關的科研工作和臨床試驗都應該恪遵醫學倫理委員會(Institutional Review Board,簡稱IRB )的監督與管理~李英雄編著,人工智慧(能)在精準醫學之實質的角色,台灣精準醫學學會網站,李怡真2018/11/27張貼。 返回內文
- 李英雄編著,人工智慧(能)在精準醫學之實質的角色,台灣精準醫學學會網站。(2019/3/12) 返回內文
- Precertification (Pre-Cert) Pilot Program: Milestones and Next https://www.fda.gov/MedicalDevices/DigitalHealth/DigitalHealthPreCertProgram/ucm584020.htm(2019/3/12) 返回內文
- FDA speeds up Artificial Intelligence Approals, Review Finds https://www.raps.org/news-and-articles/news-articles/2019/1/fda-speeds-up-artificial-intelligence-approvals-r(2019/3/12) 返回內文
- 同前註。 返回內文
- 同註12。 返回內文
- https://www.lexology.com/library/detail.aspx?g=11261474-a7f9-48b5-9c2a-f76cc9017019(2019/3/12) 返回內文
- 經濟日報https://money.udn.com/money/story/10161/3604873(2019/1/22) 返回內文
- 環球生技月刊http://www.gbimonthly.com/2018/10/33227/(2019/3/7) 返回內文
- 拜耳(Bayer)是享有超過 150 年歷史的創新公司,主要專業領域為醫療保健與作物科學。拜耳的核心事業分為三個部門經營,即西藥、保健消費品與作物科學;動物保健則為個別的事業單位。西藥部著重處方藥,特別是女性醫療保健與心臟醫學的產品,也致力於腫瘤、血液和眼科等特殊醫療領域。西藥部還包含放射醫學事業,提供必要顯影劑的對比增強診斷影像儀器。該公司在2014年收購MSD旗下保健消費品業務,在交易中達成全球可溶性鳥苷酸環化酶(sGC)調節劑以及心血管疾病治療領域的合作,目標是在未滿足醫療需求的全面評估。 https://www.bayer.com/ 返回內文
- 慢性血栓栓塞性肺高壓(Chronic thromboembolic pulmonary hypertension, CTEPH) 是一種罕見的肺動脈高壓,全球約有8至40人受影響。此為一種罕見的疾病,CTEPH常見的診斷方式是利用電腦斷層掃描以及通氣/灌注掃描(V / Q掃描)用於檢測血凝塊是否阻塞肺部血管並引起肺動脈高壓。然而CTEPH可能難以診斷,因為其症狀與其他肺部疾病相似,醫生無法準確的辨識CTEPH。 返回內文
- https://media.bayer.com/baynews/baynews.nsf/id/FDA-grants-breakthrough-device-designation-artificial-intelligence-software-CTEPH-pattern(2019/3/12) 返回內文
- 拜耳辨識栓塞性肺高壓AI軟體獲FDA突破性設備指定https://www.gbimonthly.com/2018/12/36948/?fbclid=IwAR0PRFMSIKe8U-Dy43ZBmPeb8V1M-eEgzGWHfSbFFm3_cVoO0YT4Jiy_c4s(2019/3/12) 返回內文
- 環球生技月刊https://www.gbimonthly.com/2018/12/36948/?fbclid=IwAR0PRFMSIKe8U-Dy43ZBmPeb8V1M-eEgzGWHfSbFFm3_cVoO0YT4Jiy_c4s (原文:https://media.bayer.com/baynews/baynews.nsf/id/FDA-grants-breakthrough-device-designation-artificial-intelligence-software-CTEPH-pattern)(2019/3/7) 返回內文









